الکل ها: کاربرد در صنایع
الکل خالص مایعی بی بو وبی مزه است که با استفاده از تخمیر شکر و مخمر تهیه می شود و در آبجو، شراب و نوشیدنی های الکلی استفاده می شود. الکل هم یک ماده شیمیایی است و هم یک داروی روانگردان می باشد. در علم شیمی، الکل زمانی به وجود می آید که یک گروه هیدروکسی، یک جفت اتم اکسیژن و هیدروژن، جایگزین اتم هیدروژن در یک هیدروکربن شود. الکل ها با سایر اتم ها پیوند تشکیل می دهند و الکل های ثانویه را ایجاد می کنند.
الکل ها دسته ای از ترکیبات آلی با گروه ها هیدروکسیل (-OH) هستند. متانول (الکل چوب ) سادترین الکل است که کاربرد زیادی به عنوان سوخت و حلال دارد. اتانول (الکل غلات) که با فرایند تخمیر تهیه می شود کاربرد فراوانی در صنایع بهداشتی ، آرایشی و پزشکی دارد و عنوان یک سوخت دوستدار محیط در برخی از خودروهای دوگانه سوز به کار می رود. ایزوپروپیل الکل به عنوان ضدعفونی کننده پوست پیش از تزریق به کار می رود.
در واقع الکل یک ماده آلی دارای گروه عاملی OH متصل به کربن با فرمول عمومی R–OHR–OH است. الکلها بیشترین ترکیبات آلی را شکل میدهند. در ساخت عطرها و سنتز بسیاری از ترکیبات بکار میروند. دو تا از مهمترین الکلها در جهان، متانول و اتانول هستند. از اتانول در تهیه لوازم آرایشی، داروسازی و سوختها استفاده میشود. متانول به عنوان ماده اولیه در تولید فرمالدهیدها و رزینها کاربرد دارد. همچنین از این الکل در سوختها، ضدیخ و تمیز کردن فلزات استفاده میکنند.
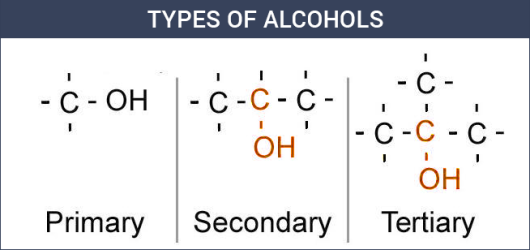
الکل ها همچنین در دستهبندی دیگری به الکلهای نوع اول، دوم و سوم تقسیم میشوند:
الکل نوع اول
اگر به کربن متصل به گروه OHOH، تنها یک گروه آلکیل متصل باشد، به آن الکل نوع اول یا الکل نوع ۱ میگویند.
الکل نوع دوم
در صورتی که دو گروه آلکیل به اتم متصل به گروه هیدروکسیل وصل شده باشند، به آن الکل نوع دوم اطلاق میشود.
الکل نوع سوم
با توجه به ترتیب ذکر شده، اگر گروههای متصل به کربن شامل سه گروه باشند، الکل مورد نظر، نوع سوم است.
حلالیت الکل ها در آب
الکل های کوچک کاملاً در آب حل می شوند. با افزایش طول زنجیره هیدروکربن در الکل، میزان حلالیت کاهش می یابد. در چهار اتم کربن و بالاتر، کاهش حلالیت قابل توجه است. اتانول را به عنوان یک الکل کوچک معمولی در نظر بگیرید. در هر دو آب خالص و اتانول خالص اصلی ترین جاذبه های بین مولکولی پیوندهای هیدروژنی هستند. برای مخلوط کردن این دو، پیوندهای هیدروژنی بین مولکول های آب و پیوندهای هیدروژنی بین مولکول های اتانول باید شکسته شوند. برای هر دوی این فرآیندها انرژی لازم است. با این حال، هنگامی که مولکول ها مخلوط می شوند، پیوندهای هیدروژنی جدیدی بین مولکول های آب و مولکول های اتانول تشکیل می شود. انرژی آزاد شده هنگام تشکیل این پیوندهای جدید هیدروژنی تقریباً انرژی مورد نیاز برای شکستن فعل و انفعالات اصلی را جبران می کند. علاوه بر این، افزایش بی نظمی سیستم، افزایش آنتروپی وجود دارد.
خواص فیزیکی الکل ها
الکل ها به دلیل توانایی ایجاد پیوند هیدروژنی نسبت به هیدروکربن ها ی مشابه دمای ذوب و جوش بالاتری دارند.توانایی تشکیل پیوند هیدروژنی موجب شده است تا الکل های با جرم مولکولی پایین به خوبی در آب حل شوند. اما با افزایش طول زنجیر هیدروکربنی انحلال پذیری الکل ها در آب کم می شود.